Interdyscyplinarne Środowiskowe Studia Doktoranckie "Fizyczne, Chemiczne i Biofizyczne Podstawy Nowoczesnych Technologii i Inżynierii Materiałowej " (FCB)
Zastosowanie enzymów jako biokatalizatorów w procesach produkcyjnych pozwala na obniżenie stosowanych temperatur i ciśnień oraz zwiększenie selektywności metody syntezy względem metod chemicznych.
 Tytuł projektu
Tytuł projektu
Interdyscyplinarne Środowiskowe Studia Doktoranckie "Fizyczne, Chemiczne i Biofizyczne Podstawy Nowoczesnych Technologii i Inżynierii Materiałowej " (FCB)
 Nazwa Beneficjenta/Beneficjentów
Nazwa Beneficjenta/Beneficjentów
Instytut Katalizy i Fizykochemii Powierzchni PAN w Krakowie
 Nazwa programu
Nazwa programu
Program Operacyjny Wiedza Edukacja Rozwój
 Konkurs
Konkurs
Interdyscyplinarne Studia Doktoranckie
 Wartość projektu
Wartość projektu
10 123 883,00 zł na 75 osób
 Wartość dofinansowania
Wartość dofinansowania
134 895,00 zł na jedną osobę
 Okres realizacji projektu
Okres realizacji projektu
1.09.2017 - 31.08.2022 (przedłużony do 31.10.2023)
Poznajcie nasz zespół
- mgr inż. Agnieszka Winiarska (doktorantka studiów FCB realizowanych w IKiFP PAN)
- prof. dr hab. Maciej Szaleniec (IKiFP)
- dr hab. Anna Bodzoń-Kułakowska, prof. AGH
- dr Joanna Kryściak-Czerwenka (IKiFP)
Zobacz efekt naszej pracy
Rezultatami badań nad oksydoreduktazą aldehydu (w skrócie AOR) z bakterii Aromatoleum aromaticum są:
- Nowy biokatalizator do selektywnej redukcji kwasów karboksylowych do aldehydów z użyciem niskich stężeń wodoru jako jedynego donora elektronów. Do produkowanych aldehydów należą m.in. wanilina, benzaldehyd, aldehyd nikotynowy, krótkie aldehydy alifatyczne.
- Nowy biokatalityczny system do regeneracji zredukowanej formy kofaktora dinukleotydu nikotynoamidoadeninowego, używanego do redukcji związków za pomocą oksydoreduktaz;
- Skonstruowanie kaskady enzymatycznej in vitro do produkcji alkoholi z kwasów karboksylowych z użyciem wodoru jako jedynego donora elektronów;
- Rozwiązanie struktury AOR za pomocą mikroskopii krioelektronowej oraz wyznaczenie części zależności struktura-funkcja kompleksu.
Wyniki projektu zostały opublikowane w czasopiśmie ACS Catalysis, vol. 13, 2022:
Tungsten Enzyme Using Hydrogen as an Electron Donor to Reduce Carboxylic Acids and NAD+
Agnieszka Winiarska, Dominik Hege, Yvonne Gemmecker, Joanna Kryściak-Czerwenka, Andreas Seubert, Johann Heider, Maciej Szaleniec
Efektem pracy są również polskie i europejskie zgłoszenia patentowe:
- A. Winiarska, J. Heider, M. Szaleniec. D. Hege, F. Arndt „Sposób enzymatycznej redukcji formy utlenionej dinukleotydu nikotynowo-adeninowego.” Polish Patent Application P.437449 (29.03.2021)
- A. Winiarska, J. Heider, M. Szaleniec. D. Hege, F. Arndt „Sposób otrzymywania aldehydów poprzez enzymatyczną redukcję kwasów karboksylowych”, Polish Patent Application P.437445 (29.03.2021)
- A. Winiarska, J. Heider, M. Szaleniec. D. Hege, F. Arndt, A.Wojtkiewicz, „A Method of Enzymatic Reduction of the Oxidized Nicotinamide Adenine Dinucleotide and Carboxylic Acids”, 2022; Vol. 4, EP22164459
Jaki problem rozwiązuje nasz projekt?
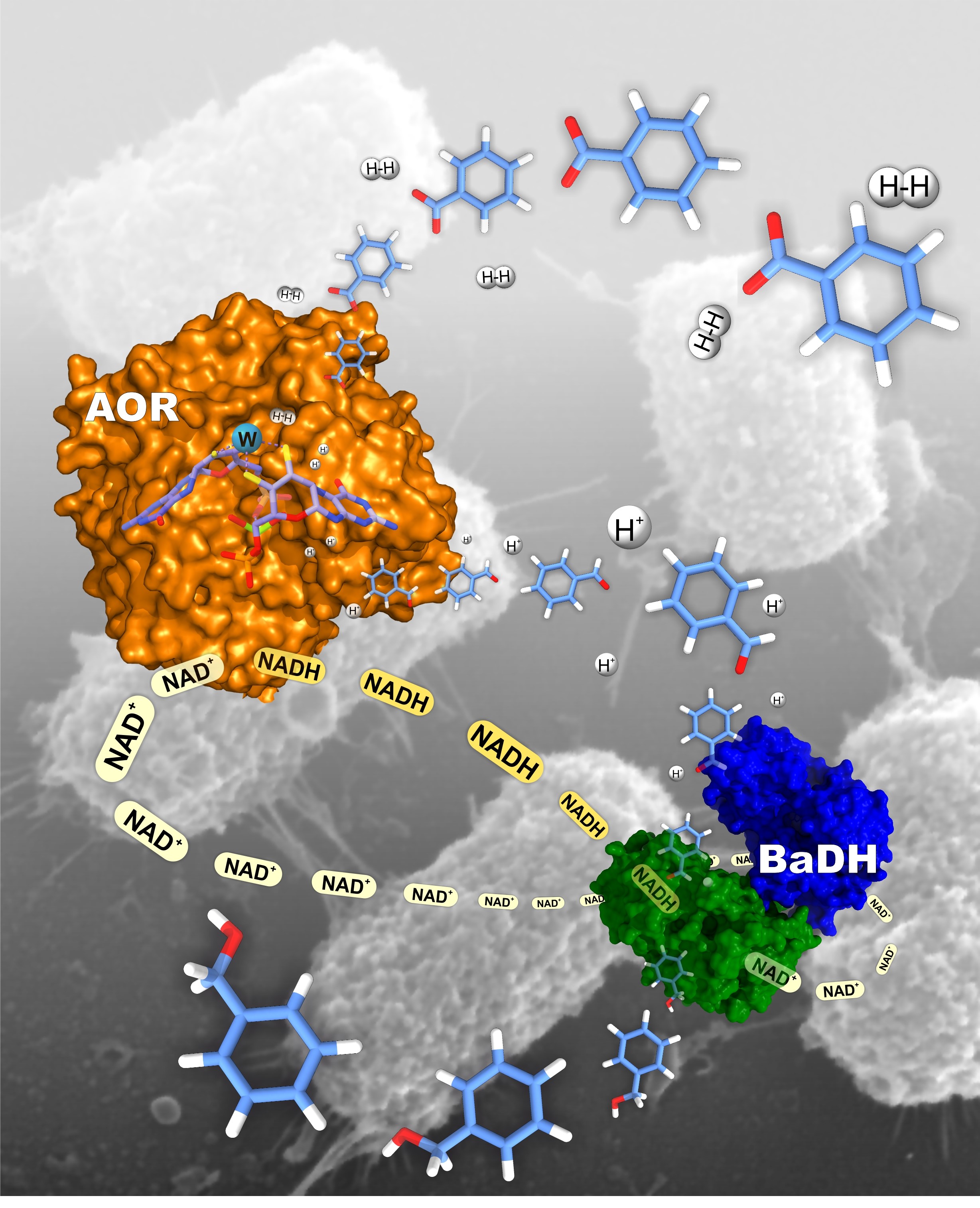
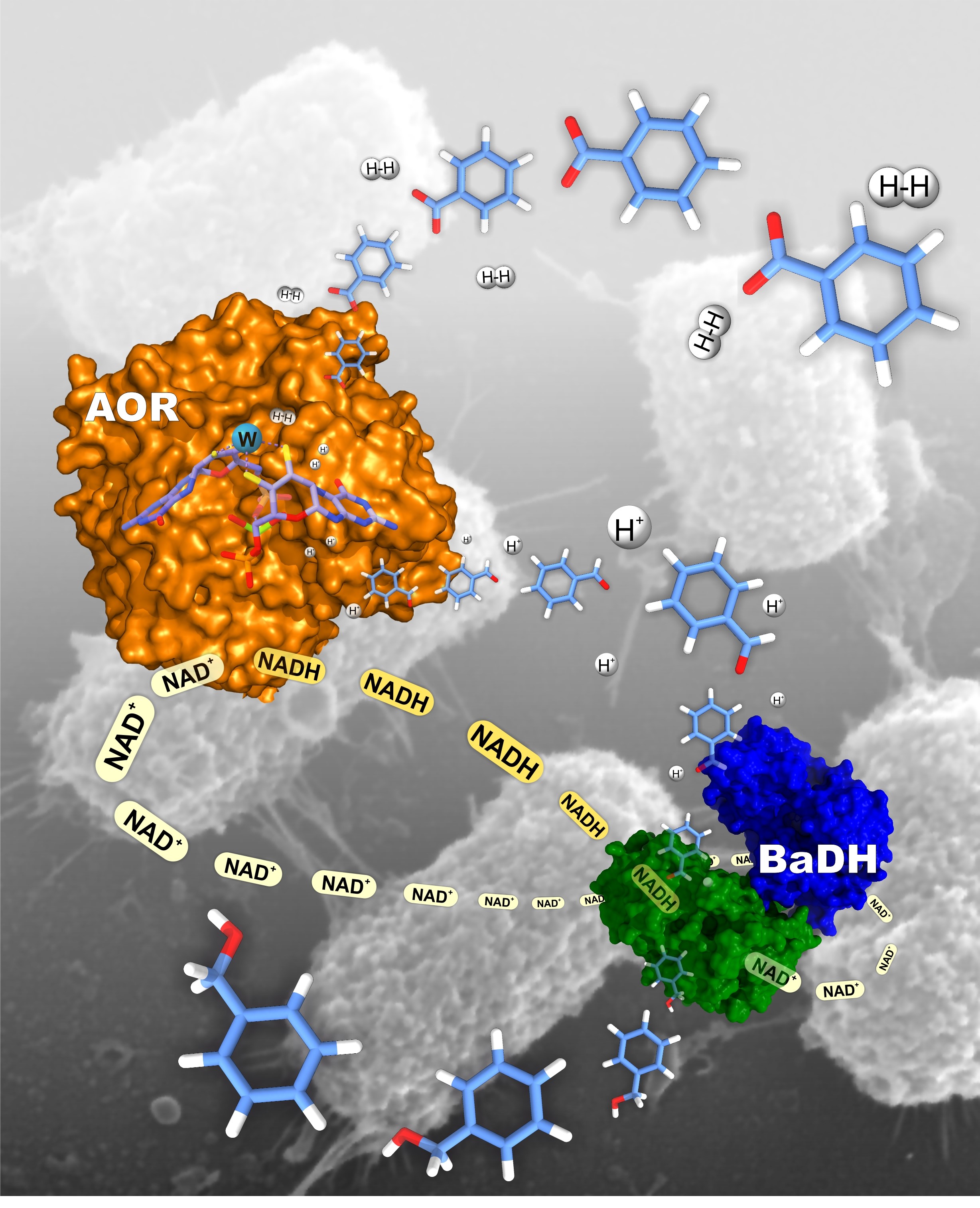
Zastosowanie enzymów jako biokatalizatorów w procesach produkcyjnych pozwala na obniżenie stosowanych temperatur i ciśnień oraz zwiększenie selektywności metody syntezy względem metod chemicznych. W efekcie procesy mogą być tańsze (mniejsze zużycie energii), a ich produkty mogą mieć mniejszy ślad węglowy i wyższą czystość. Głównym celem projektu było zastosowanie oksydoreduktaz pochodzących z bakterii Aromatoleum aromaticum do produkcji bioalkoholi z kwasów karboksylowych. Wybranymi enzymami były wolframowa oksydoreduktaza aldehydu (AOR) i dehydrogenaza alkoholu benzylowego (BaDH). Aktywności obu enzymów zostały szczegółowo zbadane, czego rezultatem było odkrycie nowej aktywności AOR jako hydrogenazy. Enzym AOR w obecności wodoru okazał się katalizować redukcję kwasów karboksylowych do aldehydów lub redukcję utlenionego dinukleotydu nikotynamidoadeninowego (NAD+) do jego zredukowanej formy (NADH).
Opracowana metoda pozwala na selektywne otrzymanie alkoholi z użyciem jedynie wodoru jako czystego i odnawialnego reduktora dla całego procesu, w którym katalizatorami były oksydoreduktaza aldehydu i dehydrogenaza alkoholowa pochodzące z bakterii Aromatoleum aromaticum.
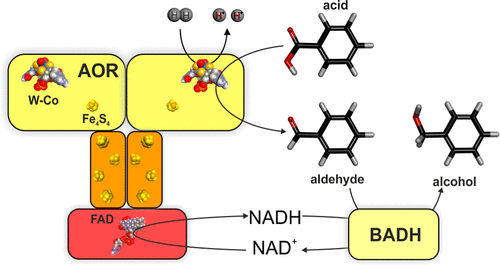
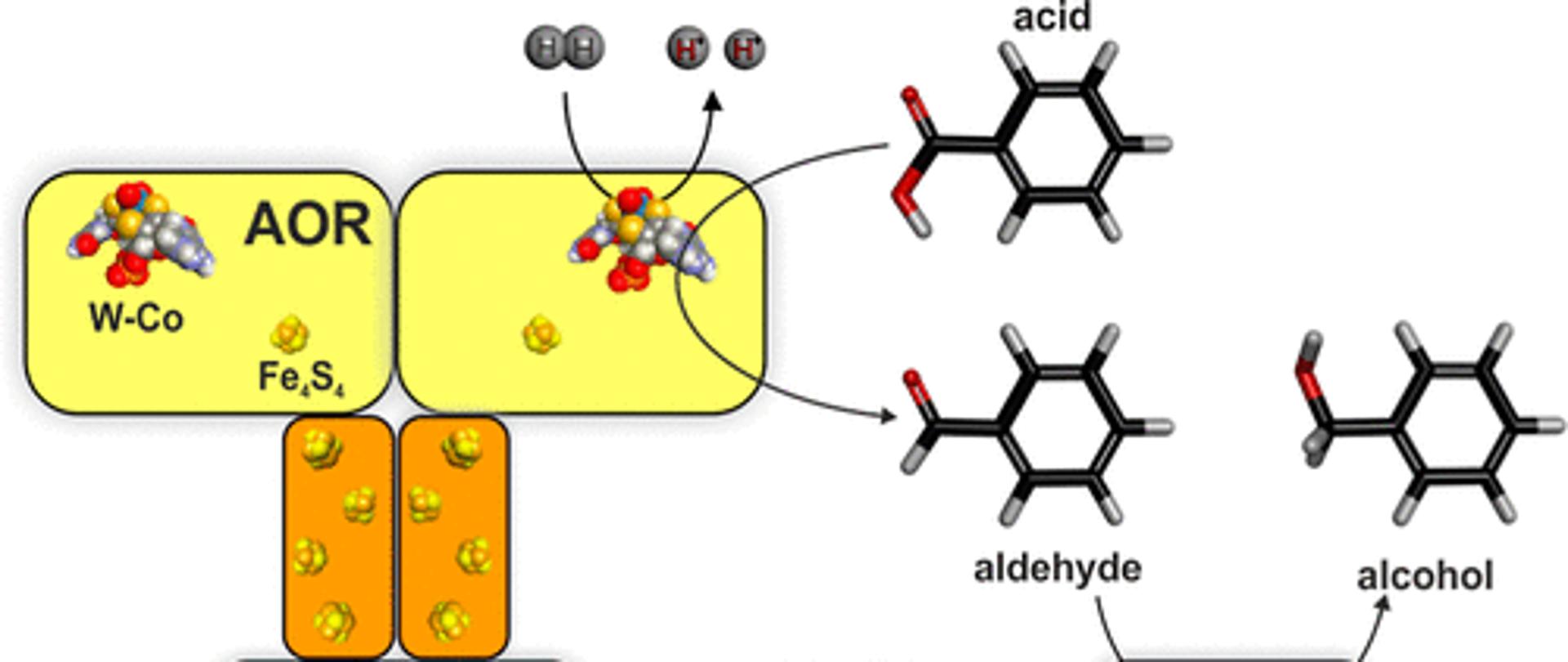
Rys 1. Schemat kaskady produkującej alkohol benzylowy z kwasu benzoesowego. BaDH wykorzystuje NADH jako donor elektronów do redukcji aldehydów.
Redukcja kwasów karboksylowych katalizowana przez AOR może być też etapem otrzymywania innych cennych związków chemicznych, dla których aldehyd jest produktem pośrednim w syntezie. Na przykład zamiana dehydrogenazy alkoholowej na aldolazę pozwoliłaby na produkcję dihydroksy-α-ketokwasów.
Enzymy wolframowe, takie jak AOR, są stosunkowo mało poznaną grupą białek. Dla części nie oznaczono jeszcze ich aktywności, a jedynie kilka struktur takich białek zostało dotychczas rozwiązanych i to z niską rozdzielczością dla najważniejszego fragmentu tj. centrum aktywnego zawierającego związany jon wolframu. Nasz projekt szczególnie przyczynił się do poznania możliwości katalitycznych i struktury AOR.
Kto korzysta/skorzysta z wyników projektu?
Nowe aktywności AOR mogą być wykorzystane w syntezie bioalkoholi, aldehydów oraz ich pochodnych wykorzystywanych w przemyśle spożywczym, farmaceutycznym oraz w nowoczesnych materiałach (tzw. high-tech). Ze względu na selektywność procesu redukcji kwasu oraz czystą metodę regeneracji NADH, AOR ma duży potencjał do zastosowania jako biokatalizator w nowych ścieżkach syntezy leków, dodatków do żywności (wanilina) i innych cennych związków.
Co było dla nas największym wyzwaniem w projekcie?
Odkryta przez nas nowa aktywność AOR jako hydrogenazy w redukcji kwasów karboksylowych to reakcja, której zachodzenie jest pozornie termodynamicznie nieprawdopodobne ze względu na dużą różnicę potencjału redukcji kwasu i utleniania wodoru. W związku z tym, udowodnienie nowej aktywności katalitycznej AOR wymagało dodatkowo dużej liczby eksperymentów, które pomogły wyjaśnić, dlaczego ta reakcja zachodzi nawet przy niskich stężeniach wodoru.
Ponadto, ze względu na wrażliwość biokatalizatora (AOR) na tlen atmosferyczny charakterystyka katalizatora i opracowanie metody syntezy aldehydu wymagało zastosowania warunków beztlenowych. Zarówno oczyszczanie biokatalizatora jak i syntezy były prowadzone w komorze beztlenowej oraz z wykorzystaniem specjalnej metodyki pracy w celu uniknięcia kontaktu z tlenem.
Określenie warunków pracy reaktora (stężenie wodoru, substratu, pH) do produkcji bioalkoholi wymagało dokładnej charakterystyki reakcji katalizowanych przez oba enzymy.
Badania struktury AOR były wyzwaniem zarówno przez wrażliwość enzymu na tlen jak i przez brak krystalizacji białka (co uniemożliwiło rozwiązanie struktury metodami dyfrakcji rentgenowskiej). W celu rozwiązania tego problemu przeprowadziliśmy badania struktury metodą mikroskopii krioelektronowej i fotometrii mas we współpracy z Centrum Synmikro w Marburgu, w Niemczech. Jednocześnie strukturę centrum aktywnego rozwiązaliśmy dokonując reinterpretacji mapy gęstości elektronowej sprzed 25 lat z AOR z P. furiosus z pomocą modelowania QM:MM. W ten sposób uzyskaną strukturę kofaktora wolframowego mogliśmy wprowadzić do naszego modelu.